Pneumologie
Publié le 14 fév 2022Lecture 11 min
Les nodules sub-solides solitaires
Robert BARBIER(1), Sopagnnha SO(2), Arnaud PFORR(3) - 1. Centre de pneumologie, clinique Rhône Durance, Avignon ; 2. Pneumologie, Centre hospitalier Henri Duffaut, Avignon ; 3. Chirurgie thoracique, Centre hospitalier Henri Duffaut, Avignon
Les nodules sub-solides (NSS) pulmonaires solitaires sont découverts de façon courante avec la multiplication des examens tomodensitométriques. Moins fréquents que les nodules solides (NS), ils témoignent bien plus souvent, quand ils sont persistants, d’une origine tumorale que les NS. Il s’agit alors assez fréquemment d’un état très précoce de l’ADC lépidique (forme pré-invasive) ou de sa forme invasive. Ces lésions ont un excellent pronostic et une évolution très lente. Certaines d’entre elles (même invasives) sont probablement totalement indolentes et exposent donc le patient au risque de surdiagnostic. Il existe plusieurs propositions de recommandations de prise en charge de ces NSS sans qu’il y ait un consensus total.
La tomodensitométrie (TDM) est l’examen du diagnostic et de la surveillance des NSS. Un nodule est une opacité focale du parenchyme pulmonaire quelle que soit sa forme mesurant entre 3 mm et 3 cm (plus grand diamètre), entourée sur au moins 2/3 de ses limites par du parenchyme pulmonaire. Le NSS a une densité inférieure aux vaisseaux qui le traversent et le laissent visible, il prend un aspect en verre dépoli (VD). Il peut contenir une part solide (PS) et on parle alors de nodule mixte ou de nodule partiellement en VD(1). La PS semble parfois moins visible en fenêtre médiastinale qu’en fenêtre parenchyme. Certains auteurs décrivent même des nodules en verre dépoli « hétérogènes » caractérisés par une PS visible en fenêtre parenchyme, mais pas en fenêtre médiastinale(2). Ce type particulier de NSS n’est pas pris en considération par les recommandations. Certains ne considèrent que la visibilité en fenêtre médiastinale de la PS(3) pour classer le NSS en nodule mixte en arguant d’un meilleur accord inter-radiologues. D’autres auteurs(4) reprochent à la fenêtre médiastinale de sous-estimer la PS et considèrent que la fenêtre parenchymateuse est mieux adaptée pour évaluer la PS d’un NSS avec un accord inter-radiologues jugé satisfaisant. Quoi qu’il en soit, même si intuitivement la PS visible en fenêtre médiastinale semble être le noyau dur d’un NSS, c’est sa partie visible en fenêtre parenchymateuse qui compte désormais (cf. infra). Les progrès techniques déjà acquis de l’imagerie permettront de dépasser ce débat.
RÈGLES D’ACQUISITION DES IMAGES
Un scanner à coupes fines (< 1,25, voire < 1 mm) pour les NSS est exigé, coupes jointives ou légèrement chevauchées permettant des reconstitutions, non injecté (sans intérêt pour la détection ou la caractérisation de nodules pulmonaires). Des coupes plus épaisses entraînent des erreurs de densitométrie du nodule et nuisent à la détection d’une composante solide de petite taille(5-7). Les reconstitutions multiplanaires permettent de repérer des images de faux nodules qui apparaissent linéaires dans certains plans. Elles permettent aussi plus de précision pour évaluer diamètre et volume. Il faut obtenir une inspiration profonde à chaque examen au risque d’observer des mesures non reproductibles de diamètre ou volume(5,6). L’acquisition avec basse irradiation est conseillée et se révèle fiable pour ces NSS pour la détection, l’évaluation des dimensions et la surveillance avec l’avantage d’une baisse de l’exposition aux rayonnements ionisants(8). L’acquisition d’images en ultra-basse dose est à l’étude pour les NSS et elle est prometteuse. Elle permettrait une réduction considérable de l’irradiation, proche de celle de la radiographie thoracique(9,10).
COMMENT MESURER UN NSS : DIAMÈTRES, VOLUMES OU MASSE ?
Si on suit les recommandations de la Fleischner Society (cf. infra), la mesure du diamètre reste encore aujourd’hui prioritaire pour les NSS. Elle se fait en fenêtre parenchymateuse : pour les nodules < 10 mm (plus grand diamètre), on retient la moyenne entre grand axe (longitudinal) et petit axe (perpendiculaire) qui reflète mieux le volume que le grand axe seul. À partir de 10 mm, les deux diamètres (longitudinal et perpendiculaire) sont notés. Le plus grand diamètre de la PS est noté si > 3 mm. On réalise les mesures sur la même orientation de coupe (axiale, coronale ou sagittale) qui donnent les plus grands diamètres. Compte tenu des aléas de mesure, on arrondit celles-ci à l’unité la plus proche, au mm supérieur pour 0,5(6).
La mesure du volume des NSS en TDM reste difficile et aléatoire et ne semble pas devoir être utilisée pour l’évaluation et la surveillance de ces nodules en dehors d’une éventuelle PS bien qu’elle soit parfois multifocale(11,12). La mesure de la masse est une voie de recherche(12,13). Certains auteurs proposent aussi de mesurer le ratio entre la dimension de la PS en fenêtre parenchymateuse (voire médiastinale) et celle de la totalité du NSS en fenêtre parenchymateuse. Ce ratio semble fortement corrélé avec le caractère invasif de la lésion(2,13).
Il est probable que, dans l’avenir, l’évaluation des nodules tirera profit des progrès techniques d’imagerie déjà accessibles : utilisation de marqueurs radiomiques comme l’histogramme des atténuations par exemple (figure 1) ou la texture, le système CAD (Computed Aided Detection – Diagnosis), l’intelligence artificielle, le deep learning...(12,14).
Figure 1. Exemple d’utilisation de marqueurs radiomiques : les histogrammes d’atténuations (reproduit d’après(12)). Les histogrammes d’atténuation (en vert) d’un adénocarcinome à invasion minime (à gauche) et d’un adénocarcinome invasif (à droite) ; la courbe en bleu correspond à une distribution de Gauss « normale ».
La mesure des diamètres reste encore la règle pour la surveillance des NSS (même si beaucoup insistent sur les volumes). Il faut aussi tenir compte des diamètres d’une éventuelle PS. Pour la Fleischner Society, c’est à partir de 2 mm (la mesure est arrondie au nombre entier en mm le plus proche) que l’on considère la variation de diamètre comme significative. Par exemple, une progression de 1,7mm doit être ramenée à 2 mm et devient significative(6).
D’autres paramètres sont également à prendre en compte même sans variation du diamètre global : l’augmentation de la densité du VD (avec parfois une diminution de taille), l’apparition d’une distorsion de scissure, l’apparition d’une PS. Ces éléments témoignent souvent d’une progression « maligne »(15).
Signification d’un NSS persistant ?
Les NSS persistants possèdent un fort potentiel de malignité.
Les NSS peuvent disparaître radiologiquement en quelques mois. Après 3 mois, ils sont dits persistants. Certains d’entre eux se révèlent malgré tout bénins après prélèvement chirurgical même quand ils possèdent une PS. Ils sont faits d’exsudat, de fibrose, d’épaississement des parois alvéolaires ou de granulome(16).
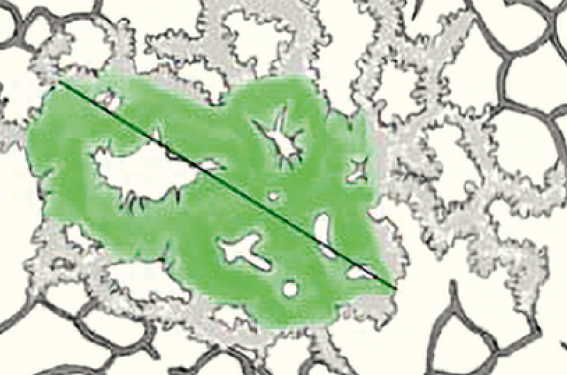
Les NSS persistants correspondent pour une très forte proportion au spectre des ADC à prédominance lépidique (APL) depuis les stades très précoces jusqu’à l’APL. Ils se singularisent par un excellent pronostic. Le VD représenterait le développement lépidique des lésions et la PS traduirait le développement invasif des lésions (figure 2).
Figure 2. Nodule mixte : l’envahissement lépidique est représenté par les parois alvéolaires épaissies et « grises » correspondant au VD décrit en radiologie ; la part « invasive » de la lésion ici représentée en vert correspond à la PS en radiologie (reproduit d’après(4)).
Une bonne corrélation anatomo-radiologique a été établie pour les lésions du spectre APL (tableau1) et a participé à la prise en charge de ces nodules(17,18).
Néanmoins, cette corrélation est loin d’être infaillible et certains ADC invasifs non lépidiques peuvent se présenter sous la forme d’un NSS totalement en VD(19). À l’inverse, la PS peut surestimer la dimension de la part invasive anatomopathologique. En effet, la PS traduit parfois un simple phénomène de collapsus alvéolaire, la présence de cellules inflammatoires(20)...
Rappelons par ailleurs les rares observations de NSS en VD purs et solitaires qui se sont révélés être la métastase par exemple d’un mélanome(21).
L’histoire naturelle des NSS appartenant au spectre des ADC à prédominance lépidique est d’une grande variabilité.
Il existe un continuum évolutif(17) entre ces différentes entités (HAA -> AIS -> AIM -> APL).
Le risque évolutif d’une forme précoce vers une forme invasive a été évalué par de nombreuses équipes. Les NSS en VD pur, voire avec une PS peuvent rester stables pendant des décennies. Il est admis que près de 20 % des NSS en VD pur vont progresser pendant la surveillance, chiffre qui passe à près de 40 % pour les NSS avec PS(14,22).
Quoi qu’il en soit, même si les NSS et particulièrement ceux avec PS ont un risque plus élevé de malignité, les NSS malins affichent un comportement bien plus indolent que les nodules totalement solides et sont moins susceptibles de donner lieu à une atteinte ganglionnaire ou à des métastases à distance(23). Les facteurs prédictifs de malignité (ou de croissance) des NSS ont été largement étudiés. Les résultats ne sont pas toujours concordants. Parmi les facteurs liés à la typologie du nodule, la progression en dimension des NSS s’accompagne à terme d’une plus forte proportion de formes invasives des lésions (AIM et APL). De même, une plus forte dimension globale initiale et une plus forte proportion de PS s’accompagnent d’une plus forte proportion de formes invasives(24). Parmi d’autres facteurs liés à la typologie du nodule, citons l’apparition d’une PS dans un NSS jusque-là en VD pur et l’existence de « bubble like lucencies » ou pseudo-cavitations (figure 3)(25).
Figure 3. Nodule mixte, contenant des « pseudo-cavitations », c’est un ADC invasif (d’après(25)).
Parmi les facteurs indépendants de la typologie du nodule, citons un ATCD de cancer du poumon ou d’un autre cancer(2,24). La consommation tabagique, alors que les NSS sont plus fréquents chez les non-fumeurs, semble bien être un facteur de risque d’évolution maligne(2). Certaines recommandations (BTS) intègrent le modèle de Brock. Un calculateur (modèle de Brock) en ligne permet d’estimer le risque de malignité d’un nodule (NSS et NS)(15,26) (figure 4).
L’étude des mutations oncogéniques présentes dans les NSS permettra de mieux comprendre les scénarios qui font qu’une simple HAA progresse vers un APL.
Figure 4. Calculateur de Brock (Brock University cancer prediction equation) permettant de prédire la malignité d’un NS ou NSS. Il exprime le risque de malignité en %.
https://www.uptodate.com/contents/calculator-solitary-pulmonary-nodule-malignancy-risk-in-adults-brock-university-cancer-prediction-equation
Certaines études ont montré que ces mutations constituaient des facteurs prédictifs d’une éventuelle progression maligne. Pour Kobayashi(2), les mutations du gène codant pour l’EGFR, mutations les plus fréquemment observées au cours des NSS, sont attachées à une plus grande fréquence de progression. À l’inverse, il rapporte que les mutations KRAS semblent présentes dans l’HAA à une fréquence bien plus importante que ce que l’on observe dans l’ADC invasif. Cela suggère que certains nodules de type HAA avec mutation KRAS doivent subir un phénomène de régression spontanée. Il en serait de même dans une certaine mesure pour la mutation BRAF. Enfin, les NSS sans mutation oncogénique (EGFR, KRAS, ALK ou HER2) semblent destinés à rester stables. Kim et coll.(18) suggèrent que la mutation EGFR (déjà très présente dans l’HAA) est un événement précoce dans la pathogenèse des ADC non mucineux. La mutation p53 ne semble pas habituelle dans les formes pré-invasives de l’ADC, mais elle progresse de l’HAA à l’ADC à PL. Son apparition serait un marqueur du caractère invasif au cours de l’évolution de ces lésions. Ceci mérite des études plus approfondies surtout à l’heure où les biopsies transthoraciques de ces nodules pourraient apporter plus d’information qu’on en espérait initialement.
Plusieurs recommandations de PEC des NSS ont été publiées ces dernières années
Les recommandations des sociétés savantes ont donné lieu à des publications accessibles facilement en ligne.
Celles de la Fleischner Society sont les plus connues(6). Elles ont été publiées en 2017 et abordent les NS et NSS « incidents ». Elles remplacent l’édition de 2013 pour les NSS.
Les recommandations de la BTS datent de 2015 et portent aussi sur les NS et NSS « incidents »(26). Les recommandations de l’ACCP datent de 2013(27). Elles ont été adaptées pour les populations asiatiques en 2016(28). L’American College of Radiology a édité des recommandations (Lung-RADS) destinées à standardiser les comptes rendus pour les patients soumis au dépistage du cancer bronchique par scanner basse irradiation. Contrairement aux autres recommandations, pas d’algorithme, mais un classement des nodules en catégories de risque de malignité, avec des propositions de prise en charge. La dernière version (Lung RADS 1.1) date de 2019(29). La synthèse des propositions Lung RADS 1.1 est accessible (https://www.acr.org/-/media/ACR/Files/RADS/Lung-RADS/LungRADSAssessmentCategoriesv1-1.pdf).
Toutes ces recommandations ont des éléments concordants, mais divergent sur certains points (tableau 2).
Elles s’adressent à des patients chez lesquels on découvre un NSS « incident » ou à des patients qui se soumettent à un dépistage de cancer bronchique. Elles ne s’adressent pas à des patients « trop jeunes ou trop âgés » et/ou avec cancer actif et/ou immunodéprimés. Nous nous intéressons exclusivement aux recommandations pour NSS solitaire.
Ces recommandations définissent le seuil de diamètre d’un NSS en dessous duquel il n’y a pas de surveillance nécessaire. Considérant qu’en dessous de ce seuil, le risque de malignité ou d’évolution maligne est trop faible (5 à 6 mm pour les recommandations les plus récentes, NSS avec ou sans PS).
Ces recommandations définissent aussi le seuil à partir duquel des explorations plus approfondies sont nécessaires pour aboutir éventuellement à une chirurgie. Une attention particulière est portée à la PS qui peut conduire en particulier à une TEP si ≥ 8 mm. La progression de la PS ou du diamètre total (même pour les NSS en VD pur) est un signe d’alerte. Contrairement aux recommandations plus anciennes (ACCP 2013) qui préconisaient une biopsie et/ou chirurgie des NSS en VD pur > 10 mm et persistant à 3 mois, il semble que la taille initiale d’un NSS en VD pur soit moins l’objet de préoccupation tant qu’il reste stable. En particulier, les recommandations de la Lung-RADS ne s’inquiètent pas ou peu d’un nodule en VD pur jusqu’à 30 mm (classé en catégorie 2 avec poursuite surveillance annuelle), voire d’une «lésion» en VD pur ≥ 30mm (classé en catégorie 3 au moment de sa découverte, surveillance TDM à 6 mois et catégorie 2 si stable ou progressant « lentement » avec comme simple corollaire une surveillance à 12 mois). La durée totale de surveillance des nodules et les échéances de surveillance ont évolué avec la connaissance que nous avons de l’histoire naturelle de ces NSS. On tend vers une surveillance d’au moins 5 ans et un espacement des scanners de surveillance en particulier pour les NSS en VD pur, chaque fois que possible pour réduire l’irradiation et ceci sans perte de chance. L’attitude adoptée face à un nodule tient compte du choix du patient, de son espérance de vie, des comorbidités et du risque de malignité. Dans les recommandations de la BTS, le risque est intégré dans l’algorithme décisionnel et évalué par le calculateur de Brock.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :


