Dermato - Allergo
Publié le 04 juil 2022Lecture 6 min
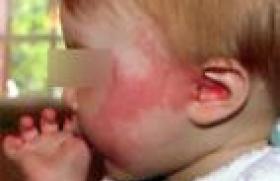
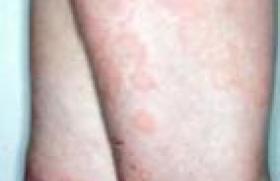
Urticaire chronique spontanée : une actualité riche
Denise CARO, Boulogne-Billancourt

La prise en charge de l’urticaire chronique spontanée (UCS) a fait récemment l’objet de deux publications importantes : les conclusions de la 6e conférence de consensus internationale qui s’est tenue à Berlin en 2020(1) et les recommandations françaises élaborées par le Centre de preuves de dermatologie également en 2020(2). L’occasion de faire le point sur l’actualité dans ce domaine.
L’UCS est une maladie dermatologique chronique inflammatoire de diagnostic clinique qui associe des papules, des angio-œdèmes et fréquemment une urticaire chronique inductible. Elle ne doit pas être confondue avec un syndrome de Wells, un syndrome de Schnitzler ou une vascularité urticarienne dont les aspects cliniques sont parfois trompeurs(3). Il est désormais admis qu’il existe principalement deux types d’UCS d’activation mastocytaire : le plus fréquent fait intervenir un mécanisme auto- immun de type-I, IgE-médié avec des auto-anticorps IgE contre des auto-antigènes du soi (anti-TPO, anti-IL24, anti-DNA…) ; le second est un mécanisme auto-immun de type-IIb, IgG-médié avec des auto-IgG (IgG anti-Fcε-RII, IgG anti-TcεRI, IgG anti-IgE)(4). Ces deux types d’UCS peuvent coexister et être en compétition l’un avec l’autre. La compréhension de ces mécanismes permet désormais de repérer les bons et mauvais répondeurs à différents traitements et de définir des biomarqueurs pour une meilleure prise en charge thérapeutique des patients.
À côté de ces mécanismes d’activation mastocytaire, il peut exister un défaut de signalisation intracellulaire ou des récepteurs de surface mastocytaire, avec des anomalies des voies activatrices ou inhibitrices (Siglec-8).
L’ÉTAPE DIAGNOSTIQUE
La conférence internationale de consensus a été l’occasion de rappeler que l’UCS n’est pas une maladie allergique et qu’un bilan allergologique n’a pas sa place, pas plus que des régimes alimentaires restrictifs. En revanche, il faut rechercher et éliminer des facteurs susceptibles de favoriser les poussées d’UCS, comme les AINS, l’aspirine ou les inhibiteurs de COX1 (le mécanisme étant pharmacologique et non allergique).
De même, un bilan minimal est indiqué pour éliminer un diagnostic différentiel (CRP élevée, hyperéosinophilie…), pour différencier les deux sous- types d’UCS (auto-IgE ou auto-IgG) et pour rechercher d’éventuelles comorbidités (30 % de dysthyroïdies). D’autres examens peuvent être demandés en fonction de l’histoire du patient et de la clinique, notamment dans les UCS anciennes et non contrôlées.
PROCÉDER PAR ÉTAPES
Les experts ont également proposé un algorithme thérapeutique comportant trois niveaux. Les anti-H1 de 2e génération sont prescrits en première intention, débutés à dose standard (environ 40 % de répondeurs), puis augmentée si besoin jusqu’à 4 fois la dose habituelle (2/3 de répondeurs).
Après 2 à 4 semaines, en cas de résultat insuffisant, on ajoute de l’omalizumab (300 mg toutes les 4 semaines). Dans les essais randomisés contrôlés, l’omalizumab obtient 36-70 % de réponses complètes, 40-60 % de réponses partielles et 3 à 8 % d’effets secondaires. En vie réelle, on a 72 % de réponses complètes, 17 % de réponses partielles et 4 % d’effets secondaires(5). En cas de non-réponse à 3 mois ou de réponse non satisfaisante à 6 mois, les experts proposent d’augmenter la dose d’omalizumab jusqu’à (600 mg) ou de raccourcir l’intervalle des prises (toutes les 2 semaines), avec 60 % de rémissions complètes ou partielles chez les non-répondeurs à la dose AMM(6).
Après 6 mois, si cela ne suffit pas, il est recommandé d’associer l’anti-H1 de 2e génération à la ciclosporine. À noter qu’il n’y a pas d’étude comparative ciclosporine/omalizumab. Toutefois l’omalizumab est mieux toléré que la ciclosporine(2).
Pour sa part, le Centre de preuves de dermatologie précise que ne sont pas recommandés faute de niveau de preuve suffisant : les anti-H2, le montélukast, les corticoïdes par voie systémique au long cours (des cures courtes peuvent être intéressantes si on ne dispose pas d’omalizumab), les immunosuppresseurs (hormis la ciclosporine), les antiinflammatoires et les immunomodulateurs, les approches psychothérapeutiques et les régimes d’éviction alimentaire systématiques(2).
Tous s’accordent à dire qu’il faut choisir un anti-H1 de 2e génération, moins sédatif et mieux toléré avec moins d’effets cholinergiques que ceux de 1re génération. Cependant, tous les anti-H1 n’ont pas été étudiés dans l’urticaire et il n’y a pas d’études comparatives entre eux. Neuf ont une AMM dans UCS (bilastine, cétirizine, desloratadine, ébastine, fexofénadine, lévocétirizine, loratadine, mizolastine et rupatadine).
Même à fortes doses, ils ont un bon profil de sécurité cardiotoxicité ; toutefois, il convient de faire attention chez les plus de 65 ans, en cas d’antécédents cardiaques et en cas d’association avec d’autres médicaments qui allongent le QT (antiarythmique, antidépresseurs tricycliques, antifongiques systémiques, neuroleptiques, prokinétiques)(7).
UNE STRATÉGIE THÉRAPEUTIQUE DE MIEUX EN MIEUX CODIFIÉE
La conférence de consensus internationale insiste sur l’importance des scores de contrôle de l’urticaire (UCT) pour adapter le traitement, l’objectif étant une rémission complète des symptômes. Un UCT < 12 correspond à une UCS non contrôlée ; il faut passer au niveau supérieur. Un UCT entre 12 et 15 est une UCS bien contrôlée ; il faut poursuivre le traitement en essayant de l’optimiser ; un UCT égal à 16 est une UCS parfaitement contrôlée ; on peut essayer de réduire le traitement(1).
Le recours à des biomarqueurs pour guider le choix thérapeutique constitue une réelle avancée dans la prise en charge des UCS. Ainsi, un taux de CRP élevé est en faveur d’une moins bonne réponse aux anti-H1. De même, un taux d’IgE de base bas (< 43 UI/mL) est associé à une réponse faible à l’omalizumab. La cinétique du taux d’IgE est importante à considérer. Un rapport IgE à 4 semaines sur IgE de base ≥ 2, est associé à une très bonne réponse à l’omalizumab(8).
En définitive, les UCS de type-I répondent mieux et plus rapidement à l’omalizumab que les UCS de type-IIb, plus souvent améliorées par la ciclosporine.
LES MOLÉCULES DANS LE PIPELINE
Enfin, différentes molécules sont en cours de développement dans l’UCS. Ainsi le ligélizumab, un anticorps monoclonal humanisé anti-IgE de haute affinité, a fait l’objet d’un essai randomisé de phase 2b pour déterminer la dose-réponse pour un contrôle des poussées à 12 semaines, puis d’une extension à 52 semaines avec 76 % de réponses cumulées. Toutefois, le taux de réponses comparé à celui obtenu avec l’omalizumab n’a pas semblé suffisamment important pour poursuivre le développement de ce médicament dans l’UCS(9).
Des anti-Siglec-8 sont également en cours de développement dans l’UCS. Dans un essai de phase 2a, le lirentilumab a montré de hauts taux de réponses complètes : 92 % chez des patients naïfs d’omalizumab, 57 % chez les patients réfractaires à l’anti-IgE et 29 % chez ceux qui avaient une réponse partielle à l’omalizumab(10).
Les cellules B constituent une autre cible d’action des médicaments. Le fénébrutinib, un inhibiteur de BTK, a été évalué chez 93 patients atteints d’UCS réfractaires aux anti-H1 (majoritairement des UCS type-IIb) dans un essai de phase 2b. À 8 semaines, 200 mg 2 fois par jour de fénébrutinib ont permis d’obtenir 56,7 % de réponses positives avec un bon profil(11).
Enfin il existe de nombreuses autres biothérapies et petites molécules en développement dans l’UCS : dans les mastocytes, des anti-IgE (quilizumab, GI-301) et un anti-Siglec-8 (CDX-0159) ; dans les éosinophiles ou les basophiles, des anti-IL5 (méplizumab, restizumab) ou anti-IL5R (benralizumab) ; dans les cellules B, un inhibiteur des CD-20 (rituximab) ; dans les T-cells, un anti-IL1 (canakinumab) ; et avec d’autres cibles comme le complément (avdoralimab) ou le TSLP (tézépélumab). Preuve que les actualités dans le traitement de l’UCS ne sont pas près de cesser.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :