Publié le 23 nov 2011Lecture 12 min
Le lambeau musculo-muqueux pédiculé sur l’artère faciale
Y. LAISSAOUI, M. ERMINY, A. BANAL, Hôpital René Huguenin-Institut Curie, Saint-Cloud
La reconstruction des pertes de substances de la cavité buccale fait appel à de nombreux procédés plus ou moins simples. Parmi ces procédés, le lambeau musculo-muqueux pédiculé sur l’artère faciale ou lambeau de FAMM (Facial Artery MusculoMucosal) occupe une place importante. Le lambeau de FAMM a été décrit initialement en 1965 par A.T. Filiberti (1), mais c’est J. Pribaz et coll.(2) en 1992 qui le font connaître pour la réparation des pertes de substances palatines transfixiantes modérées. Il s’agit d’un lambeau pédiculé sur l’artère faciale et qui est prélevé au niveau de la face interne de la joue (muqueuse + fibres musculaires du buccinateur), soit d’avant en arrière (à flux antérograde) ou d’arrière en avant (à flux rétrograde). Ses avantages, en particulier sa facilité de prélèvement, son grand axe de rotation, et le peu de complications et de séquelles du site donneur ont permis d’étendre ses indications à d’autres pertes de substances de la cavité orale voire au niveau de la fosse nasale et de l’orbite.
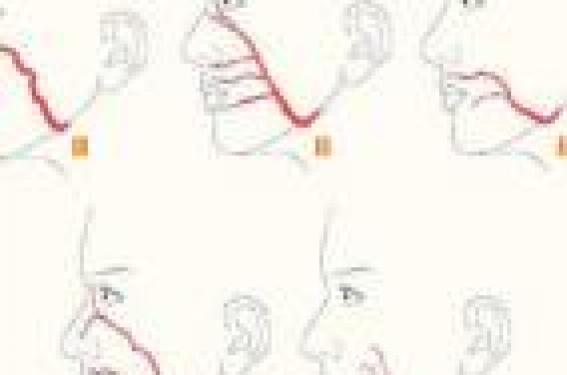
Rappels anatomiques La face interne de la joue correspond à la paroi latérale de la cavité buccale. Il s’agit d’une surface plane quadrilatère, limitée en avant par un plan frontal passant à l’aplomb de la commissure labiale, en arrière par le bord antérieur du muscle masséter, en haut et en bas par le fond du sillon gingivo-labial supérieur et inférieur. De l’intérieur vers l’extérieur, la joue comporte trois plans : la muqueuse, le plan musculaire et la peau. La muqueuse tapisse la face interne du plan musculaire profond auquel elle adhère. Elle comporte de nombreuses glandes salivaires accessoires. En regard du collet de la deuxième molaire supérieure, se trouve l’ostium du canal parotidien de Sténon. Le plan musculaire est constitué par le muscle buccinateur, muscle épais et rectangulaire et les muscles superficiels (peauciers). Entre les deux, on retrouve la boule graisseuse de Bichat, les vaisseaux et lymphatiques faciaux, le canal de Sténon, les branches du nerf facial et des branches sensitives du nerf trijumeau. La peau constitue le plan superficiel. Le lambeau de FAMM est vascularisé par l’artère faciale, collatérale de la carotide externe. Après un trajet cervical, elle contourne l’os mandibulaire au niveau de sa face caudale à la limite antérieure du muscle masséter. Au niveau du visage, elle passe à 16 mm en moyenne de la commissure labiale. Dans la région de la commissure labiale, l’artère faciale donne de nombreuses perforantes jugales ainsi que l’artère labiale supérieure. Figure 1. Terminaisons de l’artère faciale selon V. Mitz et coll. (3). 1. Artère nasale. 2. Artère angulaire. 3. Artère labiale supérieure. 4. Double. 5. Rudimentaire. Selon la classification de V. Mitz et coll. (3), elle peut terminer son parcours de 5 façons (figure 1) : – type 1 : artère nasale ; – type 2 : artère angulaire ; – type 3 : artère labiale supérieure ; – type 4 : double ; – type 5 : rudimentaire. La configuration la plus fréquemment retrouvée est le type 2. Cette artère finit son trajet sous l’appellation d’artère angulaire le long du sillon nasogénien jusqu’au cantus interne où elle s’anastomose avec l’artère dorsale du nez, issue de l’artère ethmoïdale antérieure, elle-même branche de l'artère ophtalmique. Cette disposition de l’artère faciale permet de décrire deux types de lambeaux de FAMM : le premier à pédicule antérieur dit aussi à flux rétrograde, pédiculé sur la portion distale de l’artère faciale, le deuxième à pédicule postérieur ou à flux antérograde pédiculé sur la portion proximale de cette artère. Patients et méthodes Notre travail est une étude rétrospective des dossiers de 17 patients traités à l’hôpital René Huguenin-Institut Curie, ayant bénéficié d’une reconstruction par lambeau de FAMM dans la période allant de 2005 à 2010. Nous avons analysé l’âge, le sexe et les antécédents des malades, les indications et les comptes rendus opératoires afin d’identifier les variations dans la technique chirurgicale et les suites opératoires propres à ce type de lambeau. Résultats L’âge moyen de nos patients est de 57 ans. Le sexe ratio est de 14 hommes pour 3 femmes. La majorité de nos patients a été exposée à une intoxication alcoolo-tabagique chronique (16/17), 7 patients ont des antécédents cardiovasculaires dont la gravité est variable (HTA, rétrécissement aortique, coronarite, etc.) et 4 ont une dyslipidémie. L’indication de ce lambeau était le recouvrement d’un déficit tissulaire suite à l’exérèse de cancer chez 16 patients, et le recouvrement d’une zone d’ostéoradionécrose chez un patient. Après exérèse carcinologique, la reconstruction a intéressé le plancher de bouche dans 10 cas avec recouvrement de la mandibule en cas de mandibulectomie non interruptrice. Dans 3 cas, le lambeau a comblé un déficit de la région amygdalienne, dans deux cas du voile du palais et dans un cas du vestibule. Dans notre série, 11 lambeaux sont à pédicule postérieur. Un curage ganglionnaire emportant le secteur I et conservant l'artère faciale est réalisé chez les 16 patients opérés pour un carcinome. Sur les 17 patients, une nécrose partielle est survenue chez un seul patient. Elle a intéressé la pointe du lambeau et n’a pas nécessité une reprise chirurgicale. D’autres complications moins spécifiques ont été notées telle une parotidite chez un patient. Technique chirurgicale La technique chirurgicale est décrite en plusieurs étapes. Figure 3 • Le premier temps consiste à repérer le trajet de l’artère faciale, soit à l’aide d’une sonde Doppler, soit en prenant des repères chirurgicaux systématiques (4) (bord caudal de la mandibule, bord antérieur du masséter, commissure labiale, etc.). Dans notre pratique, nous n’utilisons pas de sonde Doppler, mais en cas de curage cervical associé, nous préservons obligatoirement l’artère faciale (figure 2/illustration). • Le deuxième temps est l’exposition de la muqueuse jugale avec identification de la limite antérieure qui doit rester à 1 cm de la commissure labiale, et de la limite postérieure qui doit dépasser l’orifice de Sténon. La largeur maximale du lambeau est de 4 cm pour pouvoir effectuer une fermeture directe (figure 3). • Troisième temps : incision du lambeau après infiltration par de la xylocaïne adrénalinée à 1 %. Deux modes de prélèvement peuvent être effectués selon le sens du flux vasculaire. Figure 4. Pour le lambeau de FAMM à flux antérograde, on commence par une incision du bord postérieur qui intéresse uniquement la muqueuse, puis une incision du bord antérieur intéressant la muqueuse et le muscle buccinateur. On identifie ensuite l’artère labiale supérieure qui est liée et sectionnée, on suit le plan de cette artère (plan de l’aponévrose buccopharyngée) d’avant en arrière, jusqu'à l’artère faciale, puis on fait une incision de la limite supérieure du lambeau avec ligature et section de l’artère faciale. En cas de lambeau de FAMM à flux rétrograde, la technique est identique, mais la dissection débute au niveau du trigone rétromolaire et son point pivot est situé au niveau du sulcus gingivo-labial. La veine faciale est repérée au niveau de sa partie proximale, là où elle est la plus proche de l’artère faciale. Quand elle n’est pas individualisée, on doit garder une base large pour assurer un bon retour veineux. Le site donneur doit être fermé soigneusement en deux plans musculaires (buccinateur) et muqueux, en faisant attention à ne pas léser le canal de Sténon (figure 4). Le lambeau ayant subi une rotation et traversant le plan occlusal (fermeture du plancher buccal), le pédicule risque d’être lésé par les mouvements mandibulaires. Il doit être protégé par la mise en place d’une cale dentaire empêchant la fermeture complète de la mandibule. Cette cale doit rester en place pendant 3 à 4 semaines, jusqu’à autonomisation du lambeau, mais elle n’est pas utile en cas d’édentation (cas relativement fréquent). La section et la réinsertion du lambeau peuvent se faire sous anesthésie locale après 3 à 4 semaines, sauf chez un patient pusillanime. Figure 5. Ultérieurement, un geste de plastie peut être réalisé pour creuser le vestibule et faciliter une réhabilitation prothétique dentaire (figure 5). Indications Le lambeau de FAMM est indiqué dans la reconstruction de déficits tissulaires de taille limitée, les sites potentiels de reconstruction intéressent la cavité orale l’oropharynx, les fosses nasales, l’antre maxillaire et l’orbite (5) (tableau 1). Les processus pathologiques à l’origine du déficit sont très divers. Trois indications principales du lambeau de FAMM méritent à notre sens d’être discutées. La reconstruction primaire après chirurgie d’exérèse carcinologique Cela constitue une excellente indication de lambeaux de FAMM (5,6), tant au niveau de la fiabilité dans les suites opératoires qu’au niveau fonctionnel. P. Marandas et coll. (7) proposent désormais ce lambeau en première intention dans les reconstructions pelviennes plutôt qu’un lambeau nasogénien. T. Ayad et coll. (5) rapportent 85 % de bons résultats avec un retour à une alimentation normale, 11 % de retour à une alimentation molle et 4 % ayant recours à une sonde nasogastrique. La prise en charge de l’ostéoradionécrose La prise en charge de cette pathologie reste décevante. Aucun article ne fait directement référence et en tout cas n’évalue le lambeau de FAMM dans cette indication. En général, il est utilisé après curetage mandibulaire pour des ostéoradionécroses limitées. Pour des lésions plus avancées, il est de plus en plus souvent fait appel à un transplant microanastomosé de fibula lorsque l’état vasculaire du patient le permet (5,8) après échec d’un traitement médical bien conduit. Fermetures des communications bucco-sinusiennes Plusieurs publications font état de bons résultats dans cette indication (J. Pribaz et coll. (2), A. Joshi et coll. (9), A.K. Ashtiani et coll.(10)). Globalement, ces auteurs font état d’une excellente fiabilité de ce lambeau. Le lambeau de FAMM peut être employé aussi dans un contexte de reconstruction de déficit d’origine congénitale (fente palatine, microsmie hémifaciale), traumatique, toxique (perforation septale par usage chronique de cocaïne) et inflammatoire (maladie de Wegener) (5). Dans notre série, l’indication principale était le recouvrement de déficit tissulaire après exérèse tumorale. Nous l’avons également employé afin d’apporter du tissu sain sur des zones d’ostéoradionécrose. Au-delà des indications classiques, le lambeau de FAMM a été utilisé dans la reconstruction de déficit complexe concernant plusieurs unités faciales en association avec d’autres lambeaux (reconstruction de lèvre, menton, etc.) (9,11). Les limites du lambeau de FAMM sont, outre celles de sa taille, la section de l'artère faciale comme il est habituel de le faire dans un évidement sous-maxillaire ; cependant, les nombreuses anastomoses intrajugales, avec les axes vasculaires temporaux superficiels, maxillaires interne et mentonnier ainsi qu’avec le réseau controlatéral cervical, assurent la poursuite d’un flux antérograde de qualité (8). Le lambeau de FAMM est marqué par sa fiabilité avec une faible proportion de nécrose complète ou partielle même après radiothérapie. Le tableau 2 récapitule la fréquence de cette complication dans les différentes séries rapportées dans la littérature. On remarque que la nécrose totale est rare. Sur 194 cas rapportés dans la littérature, elle n’a été observée que dans 7 cas. La nécrose partielle est plus fréquente, observée chez 20 cas parmi 194, mais nécessite rarement une réintervention chirurgicale (2). La resensibilisation du lambeau de FAMM a été étudiée dans un travail récent de A. Wolber et coll. (14) qui ont comparé la sensibilité épicritique, au chaud et au froid, et un test pique-touche du lambeau par rapport au côté sain. Ils ont conclu à une resensibilisation quasi constante du lambeau de FAMM avec récupération d’une sensibilité de protection buccale. Le lambeau de FAMM est un lambeau facile à prélever, fiable avec une faible proportion de nécrose. Il permet la reconstruction de nombreux sites grâce à sa longueur et son grand arc de rotation. Il reste cependant limité par sa taille, et la nécessité d’une reprise chirurgicale secondaire afin de sectionner le pédicule dans certains cas. Références 1. Filiberti AT. Plastic closure of a septal perforation. Ann Chir Otorhinolaryngol 1965 ; 96 : 1-7. 2. Pribaz J et al. A new intraoral flap: facial artery musculomucosal (FAMM) flap. Plast Reconstr Surg 1992 ; 90 : 421-9. 3. Mitz V et al. Facial branches of the facial artery in adults. Typology, variations and respective cutaneous areas. Ann Chir Plast 1973 ; 18 : 339-50. 4. Dupoirieux L et al. Anatomical basis and results of the facial artery musculomucosal flap for oral reconstruction. Br J Oral Maxillofac Surg 1999 ; 37 : 25-8. 5. Ayad T et al. The musculo-mucosal facial artery flap: harvesting technique and indications. Ann Chir Plast Esthet 2008 ; 53 : 487-94. 6. Albert S et al. Reconstruction of hard palate defects using a facial artery musculomucosal flap. Ann Chir Plast Esthet 2008 ; 53 : 281-4. 7. Marandas P et al. Chirurgie des tumeurs malignes du plancher buccal : exérèse et réparation. EMC 2006 Techniques chirurgicales - Tête et cou [46-240]. 8. Marianowski R. Dix points pour faire le point sur le lambeau de FAMM, le journal faxé de l’ORL 29/05/2009 http://www.regifax.fr/journaux/pdf/9/ O190609.pdf 9. Joshi A et al. Reconstruction of intraoral defects using facial artery musculomucosal flap. Br J Plast Surg 2005 ; 58 : 1 061-6. 10. Ashtiani AK et al. Closure of complicated palatal fistula with facial artery musculomucosal flap. Plast Reconstr Surg 2005 ; 116 : 381-6 ; discussion 387-8. 11. Pribaz JJ et al. Lip and vermilion reconstruction with the facial artery musculomucosal flap. Plast Reconstr Surg 2000 ; 105 : 864-72. 12. Uglesic V, Virag M. Musculomucosal nasolabial island flaps for floor of mouth reconstruction. Br J Plast Surg 1995 ; 48 : 8-10. 13. Céruse P et al. The myo-mucosal buccinator island flap: indications and limits for the reconstruction of deficits of the buccal cavity of the oropharynx. J Otolaryngol 2006 ; 35 : 404-7. 14. Wolber A et al. Sensory function of FAMM flap: a report of 15 cases. Ann Chir Plast Esthet 2009 ; 54 : 120-5.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :





