Publié le 07 juin 2015Lecture 8 min
Une nouvelle technique de désensibilisation : l’immunothérapie épicutanée
C. THÉBAULT*, C. DUPONT** , *Directeur médical, DBV Technologies, Bagneux **Chef de service du département de pédiatrie-gastroentérologie, hôpital Necker-Enfants malades, Paris
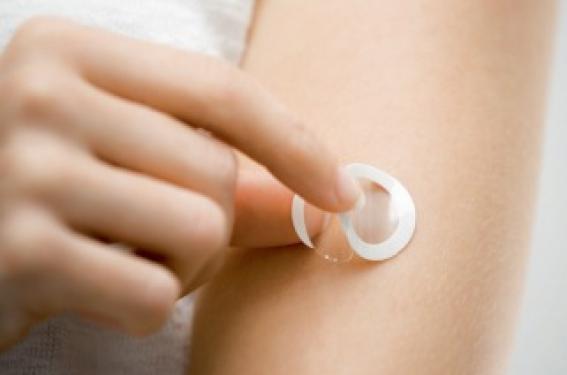
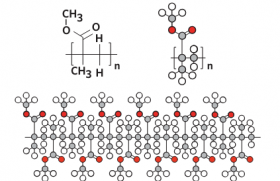
Technique en plein développement, l’immunothérapie épicutanée consiste à apposer un patch sur la peau afin de mettre en contact un allergène avec le système immunitaire de la peau et permettre ainsi une désensibilisation progressive. Ce procédé vise à traiter les allergies alimentaires, telles que les allergies à l’arachide et aux protéines de lait de vache ; il pourrait également être développé dans les allergies respiratoires aux acariens.
L’allergie alimentaire représente un problème majeur de santé chez les nourrissons et les enfants. Entre 11 et 26 millions de personnes souffrent d’allergie alimentaire en Europe et entre 220 et 520 millions de personnes dans le monde(1). Environ 8 % des enfants souffrent d’allergie alimentaire(2), 1 à 2 % d’allergie à l’arachide(3) et la prévalence de l’allergie à l’arachide chez l’enfant a presque quadruplé entre 1997 et 2008. Les allergies alimentaires (principalement à l’arachide) (tableau) sont responsables de 150 à 200 décès tous les ans aux États-Unis(4) et de plus de 125 000 admissions aux urgences(5). L’allergie à l’arachide, qui est strictement IgE médiée de type 1, représente la majorité des réactions allergiques graves liées à l’alimentation, et a tendance à se déclarer au début de la vie, sans résolution au cours du temps pour 80 % des patients allergiques et chez les personnes très sensibilisées, des traces infimes peuvent induire une réaction allergique. Jusqu’à présent, l’éviction stricte de l’aliment responsable était la seule solution proposée. La voie épicutanée Un nouveau procédé innovant visant à développer la voie épicutanée dans l’ITS (immunothérapie spécifique) – ou méthode de désensibilisation par voie épicutanée – utilisant la technologie Viaskin® a été développé. Il consiste à apposer sur la peau un patch (figure) qui met en contact l’allergène avec le système immunitaire au niveau de la surface épithéliale de la peau, en évitant son passage dans le sang. Au cours du traitement, le patch est collé sur la peau. Chez l’adulte et l’adolescent, au niveau de la partie supérieure du bras et chez l’enfant dans le dos, six zones d’application sont préalablement définies. Le patch est renouvelé tous les jours et aucune préparation spécifique de la peau (en dehors d’un simple nettoyage) n’est nécessaire. La zone d’application doit être parfaitement saine, sans blessure, ni excoriation d’aucune sorte. Les affections de la peau peuvent dans certains cas constituer une contre-indication au traitement. L’immunothérapie épicutanée (EPIT®) est développée pour augmenter le seuil de la dose réactive de l’enfant. Elle induit une désensibilisation progressive à l’allergène permettant une minimisation des réactions anaphylactiques, qui pourraient être provoquées par des expositions accidentelles à ce dernier. Après une administration à long terme de l’allergène avec le patch Viaskin®, une induction partielle ou complète de la tolérance à l’allergène est attendue. Seuls les enfants de moins de 2 ans ne sont pas, à ce stade, pris en charge, le diagnostic relevant d’un test de provocation oral. Une technologie originale La fabrication de Viaskin® fait appel à la technologie Electrospray®, un procédé inventé par DBV technologies, qui permet d’utiliser des formulations liquides pour produire des dépôts secs de substances actives chimiques ou biologiques spécifiques. N’importe quel genre de substances actives peut être pulvérisé sur ce patch, sans adjuvants, pour l’administration épicutanée. Les doses infraréactives sélectionnées, < 500 µg de protéines dans les protocoles actuels, et l’application de l’allergène sur une peau intacte suppriment tout risque de réaction générale. Un développement clinique ambitieux En 2010, une preuve de concept clinique a été obtenue dans une étude pilote chez 18 enfants de moins de 8 ans présentant une allergie aux protéines de lait de vache(7). Les patchs étaient appliqués pendant 48 h sur le dos, 3 fois par semaine pendant la phase clinique de 3 mois. Bien qu’un eczéma local puisse être induit par l’application du patch, sa régression s’observe dès le retrait de ce dernier, et la sécurité globale a pu être qualifiée de très satisfaisante. La dose cumulée réactive tolérée de lait lors des tests a été augmentée fortement à 3 mois chez certains enfants mais globalement de façon non statistiquement significative dans la petite cohorte sous traitement, avec une dose d’allergène relativement faible de l’ordre de 150 µg de protéines de lait. De la preuve de tolérance… Lors de la phase Ib de Viaskin® Peanut, étude sur la sécurité d’emploi et sur la tolérabilité de l’administration épicutanée répétée des Viaskin® Peanut sur la peau de patients allergiques à l’arachide, 100 sujets allergiques à l’arachide, dont 70 avec une allergie non sévère et 30 avec une allergie sévère, ont été randomisés et traités pendant 2 semaines par Viaskin® avec des doses de protéines d’arachide allant de 20 µg à 500 µg par patch ou par des patchs placebos. Un excellent taux d’observance du traitement (> 96 %) a été constaté et les résultats montrent que Viaskin® Peanut présente une sécurité d’emploi satisfaisante chez tous les patients allergiques à l’arachide. … à la preuve d’efficacité Une première étude de désensibilisation randomisée a été menée sur l’allergie à l’arachide (étude ARACHILD, promotion APHP), réalisée chez 54 enfants et adolescents présentant une allergie à l’arachide sévère (réactifs à moins d’une cacahuète soit 300 mg de protéines d’arachide), âgés de 5 à 17 ans. La sécurité d’utilisation a été bonne, de même que l’efficacité d’une dose quotidienne de 100 µg de protéine d’arachide, avec deux tiers de la sous-population des enfants augmentant d’au moins 10 fois leur seuil de réactivité à l’arachide à 18 mois. Cette étude se poursuit sur une durée totale de 36 mois. D’autres études cliniques sont en cours, selon le même schéma thérapeutique mais avec des doses différentes d’allergènes. L’avantage de cette technique est qu’elle évite tout contact oral ou digestif avec l’allergène, supprimant ainsi tout risque de réaction digestive ou générale lors du traitement de désensibilisation. Une phase IIb internationale a été initiée en août 2012 afin d’évaluer l’efficacité de Viaskin® Peanut sur plusieurs centaines de patients allergiques à l’arachide. Cette étude, appelée VIPES (Viaskin® Peanut Efficacy and Safety) a inclus 221 adultes et enfants, âgés de 6 à 65 ans, qui ont eu une réaction allergique objective à l’arachide après avoir consommé une dose ≤ 300 mg de protéines d’arachide (soit l’équivalent d’une cacahuète) lors du test de provocation oral initial en double aveugle contre placebo (TPODAVP). L’étude permet de tester trois dosages : 50 µg, 100 µg, 250 µg versus placebo. Tout en évaluant l’efficacité et la sécurité de Viaskin® Peanut, l’objectif final de cette étude est la sélection de la dose présentant le meilleur rapport bénéfice thérapeutique/risque. Le test de provocation orale (TPO) à l’arachide mené en double aveugle et contrôlé versus placebo (TPODAVP) est réalisé pour évaluer l’efficacité du traitement avant et après une période de traitement de 12 mois. Il s’agit d’une étude potentiellement pivot pour l’enregistrement du produit. Cette étude est suivie par une étude ouverte OLFUS (Open-Label Follow-Up Study), étude de phase IIb, qui évalue l’efficacité à long terme et l’innocuité de Viaskin® Peanut. Enfin, aux États-Unis, le Consortium for Food Allergy Research (CoFAR) a également débuté en octobre 2013 une étude multicentrique de phase II, randomisée, en double aveugle versus placebo, avec administration quotidienne de Viaskin® Peanut pour traiter les enfants et les adultes allergiques à l’arachide. Ces techniques d’immunothérapie ont profondément transformé les perspectives à court et à moyen termes des patients allergiques, permettant de passer d’une observation passive des consommations accidentelles à une phase plus active au cours de laquelle les tentatives thérapeutiques se multiplient. Toutefois, ces traitements sont encore en phase expérimentale. L’immunothérapie par voie sublinguale est basée sur la consommation orale de l’allergène, sous format non pharmaceutique, et ne peut être mise en œuvre actuellement que par des groupes spécialisés. L’EPIT® est en phase d’étude clinique avancée en vue d’en faire un traitement pharmaceutique commercialisable.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :