Rhinologie
Publié le 14 oct 2021Lecture 9 min
Polypose nasosinusienne et asthme : du lien physiopathologique au lien thérapeutique
Geoffrey MORTUAIRE, Pr. des universités-praticien hospitalier, service d’oto-rhino-laryngologie et de chirurgie cervico-faciale ;
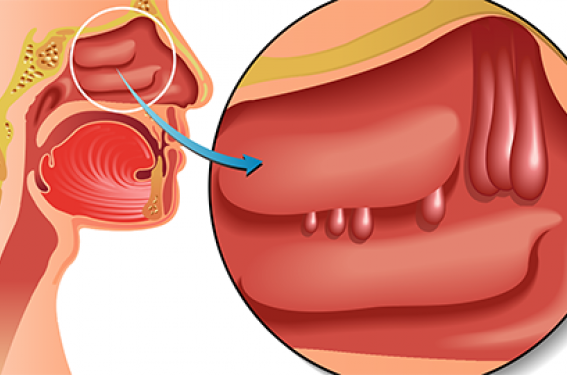
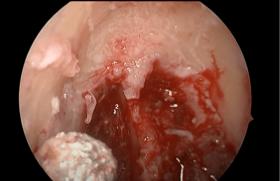
La polypose nasosinusienne (PNS) appartient au groupe des rhino-sinusites chroniques diffuses inflammatoires. Dans les pays occidentaux, la PNS se caractérise le plus souvent par une signature immunitaire de type Th2 (T2), en particulier chez les patients présentant un asthme associé. La présence conjointe d’une PNS et d’un asthme détermine des formes cliniques plus sévères et plus difficiles à traiter. La compréhension de ce lien physiopathologique et clinique est essentielle à l’identification des endotypes biologiques qui unissent ces deux pathologies respiratoires. Les enjeux sont à terme de mieux préciser la place des biothérapies dans le traitement des formes réfractaires de PNS et d’asthme associés.
LIEN ÉPIDÉMIOLOGIQUE
La PNS touche 2 à 4 % de la population générale et s’accompagne d’une altération significative de la qualité de vie avec des conséquences socio-économiques non négligeables (absentéisme professionnel, baisse de productivité, consommation de soins)(1). Un asthme de début précoce ou tardif (après 40 ans) est observé dans 40 à 67 % des cas(2) (figure 1). Cet asthme peut longtemps rester méconnu alors qu’il peut se révéler modéré à sévère dans plus de 40 % des cas(3). La triade de Widal est un phénotype clinique particulier associant une PNS, un asthme et une intolérance aux anti-inflammatoires non stéroïdiens (AINS) et à l’acide acétylsalicylique. En inhibant l’action enzymatique de la cyclooxygénase-1 (COX-1), les AINS modifient le métabolisme de l’acide arachidonique. Cela est responsable d’un déséquilibre de production entre leucotriènes et prostaglandines à l’origine d’une inflammation muqueuse accrue et de phénomènes de broncho- constriction. Ce syndrome est observé dans 15 % des PNS(4). La présence conjointe d’un asthme ou d’une triade de Widal détermine des phénotypes cliniques de PNS plus sévères(1).
Chez les patients suivis pour asthme, une PNS est diagnostiquée dans 15 % des cas. Une intolérance aux AINS est identifiée chez 7 % des patients asthmatiques, et plus particulièrement dans les formes sévères(5). Le tableau clinique de PNS et d’asthme se manifeste alors plus précocement dès l’âge de 30 ans. L’allergie respiratoire aux pneumallergènes, observée dans 12 à 20 % des PNS, ne semble pas jouer un rôle physiopathologique essentiel dans la PNS participe à l’aggravation de l’inflammation muqueuse.
Figure 1. Proportion relative des patients présentant une polypose nasosinusienne et/ou un asthme. Chez les patients asthmatiques, une polypose nasosinusienne (PNS) est observée dans environ 15 % des cas, une triade de Widal dans 7 % des cas. Chez les patients avec une polypose nasosinusienne, un asthme est observé dans environ 40 % des cas, une triade de Widal dans 15 % des cas.
LIEN PHYSIOPATHOLOGIQUE
De nombreux travaux ont permis de mieux comprendre les mécanismes physiopathologiques observés conjointement dans la PNS et l’asthme. L’association de ces deux pathologies détermine le plus souvent un profil inflammatoire tissulaire riche en polynucléaires éosinophiles (figure 2). Brièvement, l’agression de l’épithélium respiratoire par des irritants exogènes ou des pathogènes (Staphylococcus aureus) provoque la production d’alarmines (TSLP, interleukine[IL]-25, IL-33) à l’origine d’une cascade inflammatoire mettant en jeu la voie immunitaire adaptative dépendante des lymphocytes T helper de type 2 (Th2) et les cellules lymphoïdes innées de type 2 (ILC2), effectrices de la réponse innée dépourvue de récepteurs spécifiques aux antigènes (figure 1). La production de cytokines pro-inflammatoires (IL-5, IL-4 et IL-13) et de chimiokines (RANTES, éotaxines) permet le recrutement, l’activation et la dégranulation des éosinophiles, la production polyclonale d’IgE par les lymphocytes B et la dégranulation des mastocytes. Les protéines cytotoxiques ainsi libérées participent au remodelage tissulaire, à l’entretien de la réaction inflammatoire locale et à l’hyperplasie sécrétoire observés dans la PNS et l’asthme(7). Dans les pays occidentaux, ce profil Th2 dit « T2 » est observé dans 80 % des cas de PNS, surtout en association à l’asthme, tandis qu’un profil immunitaire Th1 et/ou Th17 dit « T1 » est davantage observé dans la population asiatique présentant une rhino-sinusite chronique associée ou non à l’asthme (8).
Figure 2. Voie inflammatoire de type 2 dans la polypose nasosinusienne et l’asthme. Les cellules présentatrices d’antigènes (CPA) et les alarmines épithéliales (IL-25, IL-33 et TSLP) initient la voie immunitaire lymphocytaire Th2. Les cellules effectrices (lymphocyte Th2 [Th2], lymphocyte B [LyB], cellules lymphoïdes innées de type 2 [ILC2)) expriment à leur surface les récepteurs des interleukines IL-4 et IL-13 (IL-4R/IL-13R) et des alarmines (TSLP-R). Les polynucléaires éosinophiles (EO) expriment le récepteur aux éotaxines (CCR3) et à l’IL-5 (IL-5Ra) pour leur recrutement sanguin et leur activation. Les mastocytes et les polynucléaires basophiles (baso) expriment le récepteur FC RI permettant d’interagir avec les IgE.
LIEN CLINIQUE
L’association de la PNS et de l’asthme implique que les collaborations entre ORL et pneumologue soient fluidifiées avec un examen concerté et standardisé de l’ensemble des voies respiratoires.
La prédominance des signes fonctionnels rhinologiques (obstruction, troubles de l’odorat, rhinorrhées) place souvent au second plan des signes respiratoires qu’il convient de rechercher systématiquement (toux, sifflements, dyspnée, prurit pharyngé). Un examen auprès du pneumologue est particulièrement nécessaire avant toute intervention chirurgicale nasosinusienne afin de s’assurer du bon contrôle de la fonction ventilatoire lors d’une anesthésie générale.
En cas d’asthme difficile, la recherche de facteurs locaux nasosinusiens susceptibles de déstabiliser le contrôle de la fonction ventilatoire est aussi indispensable. L’identification d’une PNS, d’une rhinite chronique ou d’une autre pathologie nasosinusienne permet de mieux phénotyper l’asthme qu’il soit allergique ou non. Cette évaluation rhinologique permet aussi de mettre en œuvre le traitement des comorbidités nasales et de réduire le palier de traitement d’un asthme parfois considéré par excès comme sévère, faute d’un contrôle satisfaisant de l’inflammation des voies respiratoires hautes.
LIEN THÉRAPEUTIQUE
La présence conjointe d’une PNS et d’un asthme a un impact péjoratif sur l’efficacité des traitements pour chacune de ces pathologies.
Le traitement de la PNS est en premier lieu médical. Les irrigations nasales répétées par des solutions salines permettent d’améliorer le drainage mucociliaire. La corticothérapie locale en spray, en solution ou en nébulisation a pour objectif de réduire l’œdème muqueux, d’améliorer l’obstruction nasale, les troubles olfactifs et globalement la qualité de vie des patients. La corticothérapie générale est proposée de manière raisonnée, en cure courte de 7 à 10 jours à la dose de 1 mg/kg/j au maximum 2 à 3 fois par an. Ce traitement est efficace pour réduire la taille des polypes, mais son usage doit être limité en raison d’effets indésirables potentiellement graves(9). Les traitements médicaux de la PNS montrent leur efficacité chez la plupart des patients avec néanmoins un risque accru d’échec sur le contrôle des symptômes nasosinusiens en présence d’un asthme ou d’un Widal. En cas d’échec du traitement médical sur l’amélioration des symptômes, un traitement chirurgical dit fonctionnel est proposé. Celui-ci consiste en une ablation des polypes associée éventuellement à une ouverture par voie endoscopique des cavités nasosinusiennes pour permettre une meilleure diffusion des corticoïdes locaux. De nouveau, la présence d’un asthme ou d’un Widal est associée à un risque plus élevé de rechutes nécessitant une nouvelle intervention pour révision chirurgicale(10).
La prise en charge de l’asthme répond aux paliers thérapeutiques définis par les guidelines du GINA (Global Initiative for Asthma). Le traitement conjoint des comorbidités nasosinusiennes comme la PNS a théoriquement pour objectif d’améliorer le contrôle de l’asthme et d’éviter une escalade thérapeutique souvent liée à une cortico-dépendance. L’impact du traitement médical de la PNS sur l’asthme est difficile à établir(11). Concernant le traitement chirurgical de la PNS, une métaanalyse publiée en 2013 montrait globalement une amélioration des symptômes respiratoires des patients asthmatiques sans modification des paramètres ventilatoires mesurés par les épreuves fonctionnelles.
L’émergence des biothérapies a permis de modifier le traitement des patients asthmatiques sévères. Les molécules actuellement disponibles ciblent principalement la voie inflammatoire T2 avec des anticorps dirigés contre les IgE (omalizu-mab), l’IL-5 et son récepteur (mépolizumab, benralizumab) et le récepteur de l’IL-4 et l’IL- 13 (dupilumab). Les études de phase III réalisées dans l’asthme soulignent l’efficacité de ces biothérapies sur le nombre d’exacerbations, la qualité de vie, la consommation de traitement symptomatique et la capacité à obtenir une épargne cortisonique(12). Les analyses de sous-groupes dans les essais menés avec le dupilumab et le benralizumab montrent une plus grande efficacité sur les paramètres de contrôle de l’asthme chez les patients présentant de manière conjointe une rhino-sinusite chronique. Cet effet peut s’expliquer par une composante inflammatoire T2 plus prononcée en cas d’asthme associé à une rhino-sinusite. Elle peut aussi s’expliquer par une réduction conjointe de l’inflammation nasale conduisant à une plus grande amélioration des symptômes et de la qualité de vie. Les résultats positifs observés dans l’asthme ont incité l’industrie à évaluer l’efficacité des biothérapies dans la PNS. Repris dans une revue récente, les essais randomisés contrôlés contre placebo menés avec l’omalizumab, le mépolizumab et le dupilumab dans la PNS ont montré une amélioration significative de la taille des polypes, des opacités sinusiennes mesurées en imagerie, de la fonction olfactive et de la qualité de vie(13).
L’effet était comparable pour le dupilumab, quel que soit le statut asthmatique des patients. Le bénéfice sur la taille des polypes était qualitativement plus important avec l’omalizumab et le mépolizumab en cas d’asthme associé ou de Widal. Le dupilumab, l’omalizumab et le mépolizumab permettaient aussi de retarder le recours à la chirurgie chez les patients atteints de PNS réfractaire au traitement corticoïde. Les résultats de l’essai de phase III portant sur le benralizumab dans la PNS seront prochainement publiés.
PERSPECTIVES ET CONCLUSION
Les données récentes obtenues avec les biothérapies modifient le paradigme de traitement de la PNS. Elles influencent aussi le bilan préthérapeutique par biothérapie dans l’asthme en soulignant l’importance de rechercher une rhino-sinusite chronique associée. Les déterminants du contrôle de la PNS et de l’asthme doivent ainsi être considérés simultanément pour optimiser les stratégies de traitement. Les réunions pluridisciplinaires de concertation thérapeutique dans l’asthme sont ainsi un bon moyen d’échange entre les deux spécialités.
Les résultats très satisfaisants des biothérapies dans les essais de phase III doivent néanmoins être mis en balance avec les expériences de terrain retrouvant parfois une efficacité thérapeutique dissociée sur le versant pulmonaire et le versant nasal. Un contrôle satisfaisant de l’asthme obtenu avec une biothérapie doit-il être remis en question si le patient n’est pas amélioré pour sa PNS ? Cela justifie-t-il de modifier la biothérapie au profit de la PNS au risque de déstabiliser le contrôle de l’asthme ? Ces questions viendront enrichir les discussions que les ORL et pneumologues doivent entretenir. Les analyses cliniques menées en vie réelle dans l’asthme (cohorte RAMSES) et prochainement dans la PNS pourront aussi fournir d’éventuels indices de compréhension.
Enfin l’approche phénotypique clinique doit s’enrichir d’une caractérisation endotypique biologique des patients afin de cerner les profils inflammatoires les plus susceptibles de bénéficier de tel protocole de soins classiques (médical ou chirurgical) ou de telle biothérapie. L’importance de mesurer les paramètres biologiques associés au profil T2 (IL-5, IgE, ECP, EDN) et de caractériser le profil d’activation des éosinophiles au niveau sanguin et tissulaire a été démontrée(14). Ces voies de recherche doivent continuer à être développées et soutenues pour permettre à terme une caractérisation précise des patients PNS et/ou asthmatiques exploitable en routine clinique.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :